強生公司 (紐約證券交易所代碼:JNJ) 今天宣布, FDA 批準(zhǔn)了其吉西他濱膀胱內(nèi)給藥系統(tǒng)Inlexzo����。

膀胱內(nèi)吉西他濱釋放系統(tǒng)���,以前稱為TAR-200, 用 于 治療卡介苗 (BCG)無反應(yīng)的高危非肌層浸潤性膀胱癌 (HR-NMIBC) 伴原位癌 (CIS) 患者,伴或不伴狀腫瘤。
醫(yī)療保健專業(yè)人員使用共同包裝的尿路置入導(dǎo)管將TAR-200 放入膀胱����。該手術(shù)在門診環(huán)境中進行,時間不到五分鐘���,無需全身麻醉或進一步監(jiān)測��。Inlexzo每個治療周期在膀胱中停留三周�,最多14個周期��。
據(jù)強生稱��,它是第一個也是唯—一個將癌癥藥物延長局部輸送到膀胱的膀胱內(nèi)藥物釋放系統(tǒng) (iDRS)�����。
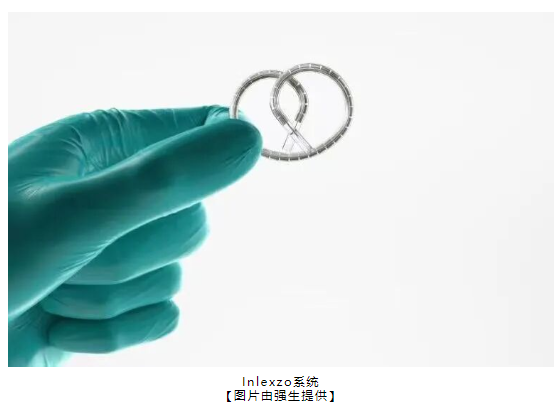
強生稱 Inlexzo 是一種可能改變實踐的方法���,用于治療 某些類型的膀胱癌�。今年早些時候�����,F(xiàn)DA 對該系統(tǒng)的一項新藥申請 (NDA) 進行了優(yōu)先審查。
2b 期 SunRISe-1 研究顯示出82.4%的完全緩解率�����,支 持 FDA 的批準(zhǔn)�����。超過一半(52 .9%)的患者在達到完 全緩解后至少一年或更長時間內(nèi)保持無癌狀態(tài)���。強生指出�����,大多數(shù)不良反應(yīng)被證明是輕度和中度的����。
強生創(chuàng)新醫(yī)學(xué)研發(fā)副總裁John Reed博士表示:“我們?yōu)閷⑽覀儙У竭@一歷史性時刻的科學(xué)感到自豪 ����,Inlexzo 是一種具有強大療效和已證明安全性的新型療法。作為唯——家同時托管藥品和醫(yī)療器械的大型醫(yī)療保健公司����,我們利用強生公司的速度和規(guī)模來加速創(chuàng)新,并為患者提供這一重要的療法 ����。




 17312606166
17312606166